在1979年,Peled提出电极电解质界面相(electrode electrolyte interphase,EEI)的概念。它是指电解液在充放电过程中分解后沉积在电极表面的一层副产物膜,在负极侧形成的EEI通常被称为固体电解质界面相(solid electrolyte interphase,SEI膜),在正极侧形成的EEI则被称为正极电解质界面相(cathode electrolyte interphase,CEI膜)。Goodenough等人从电子能量的角度解释了SEI/CEI膜的形成机理。
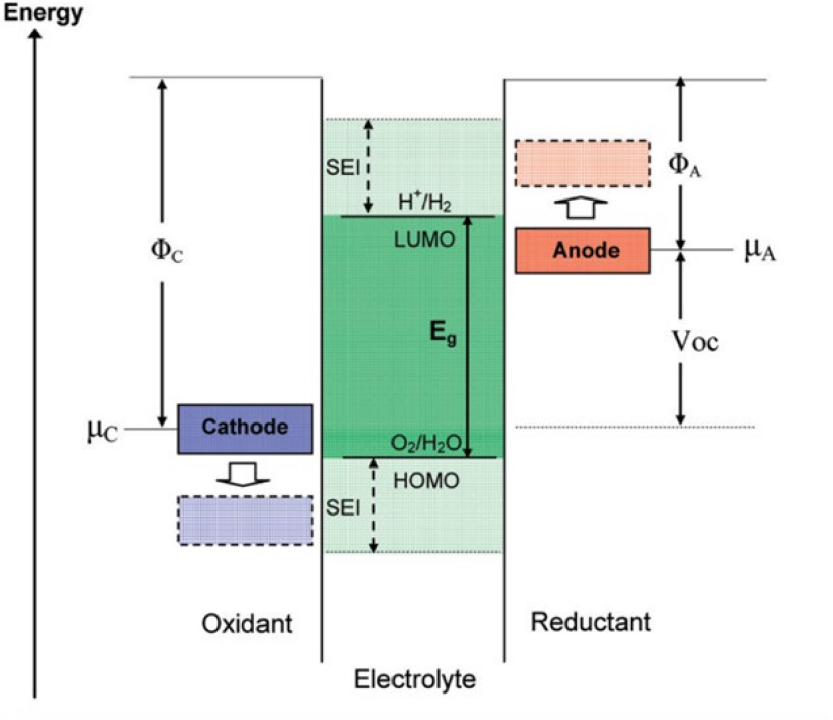
图1. SEI 电极中各组分的电子能级关系图
如图1所示,μA、μc分别代表负极、正极的化学势。当负极的化学势高于电解液组分的最低未占据轨道(LUMO)能级时,电解液组分将得到电子发生还原反应;当正极的化学势小于电解液组分的最高占据轨道(HOMO)能级时,电解液组分将失去电子发生氧化反应。电解液组分的LUMO能级与HOMO能级的能量差便是电解液组分的电化学窗口,如果电极电位位于电解液的电化学窗口内,电解液就不会在电极表面发生氧化还原反应。然而,目前常用电解液的电化学窗口较窄(图2所示),难以覆盖锂离子电池的工作电压,尤其是当使用金属Li负极和高电压正极材料时,很难避免地会形成SEI/CEI膜。为了尽可能地抑制电解液的副反应,SEI/CEI膜应具备以下特征:
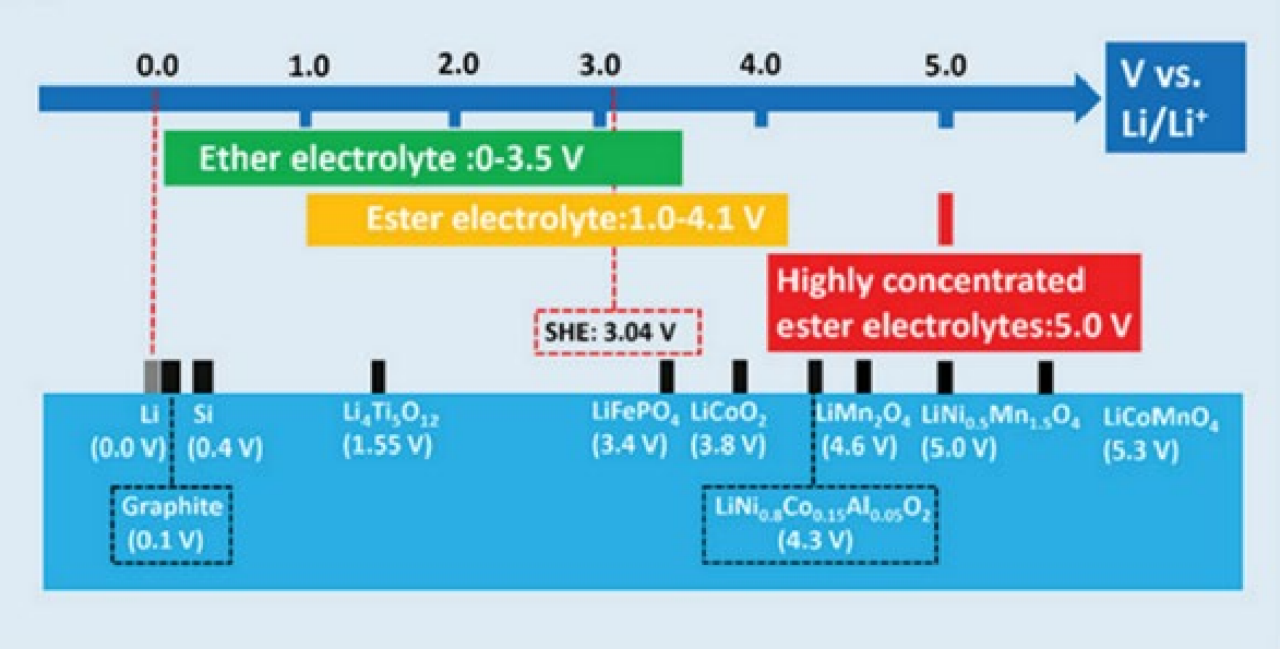
图2 部分常见的电解液的化学窗口
1)高度电子绝缘,能够阻断电解液分解的电荷转移路径,避免持续发生副反应;2)具有较高的离子电导率,有利于L计的快速传输;
3)具有良好的热稳定性与电化学稳定性,一旦形成便保持稳定,不易溶解或分解。
4)具有良好的机械性能(包含强度、韧性),能适应充放电过程中电极的体积变化,不易破裂或脱落。
5)成分/结构均匀性好,有利于L的均匀传输。
SEI/CEI膜通常为有机-无机复合物,厚度在几纳米到几百纳米间,具体成分与结构与所用电解液体系、温度、循环条件和电极材料密切相关。目前主要有两种模型描述SEI/CEI膜的结构:马赛克模型与层状模型。在马赛克模型中,无机组分随机地镶嵌在有机组分基底中[56];在层状模型中,内层主要由无机组分组成,外层主要由有机组分组成。科学研究者利用冷冻电镜发现在碳酸酯电解液中添加氟代碳酸乙烯酯(FEC)可以使金属Li表面SEI膜由马赛克结构转变为层状结构,而内层主要为非晶的有机组分,外层为Li2O晶粒。他们相信这种层状结构SEI膜有利于Li均匀传输,抑制死Li的形成。
在SEI/CEI膜形成之前,在电极/电解液界面处会形成双电层结构。在1853年Helmholt首先提出“双电层”的概念:他认为带电电极可以吸引电解液中带相反电荷的离子紧密地聚集在电极/电解液界面,但没有考虑热运动的影响。Stern等人进一步修正了该模型,将双电层结构细化为紧密层和扩散层(图3),分别命名为内亥姆霍兹(IHP)与外亥姆霍兹层(OHP)。
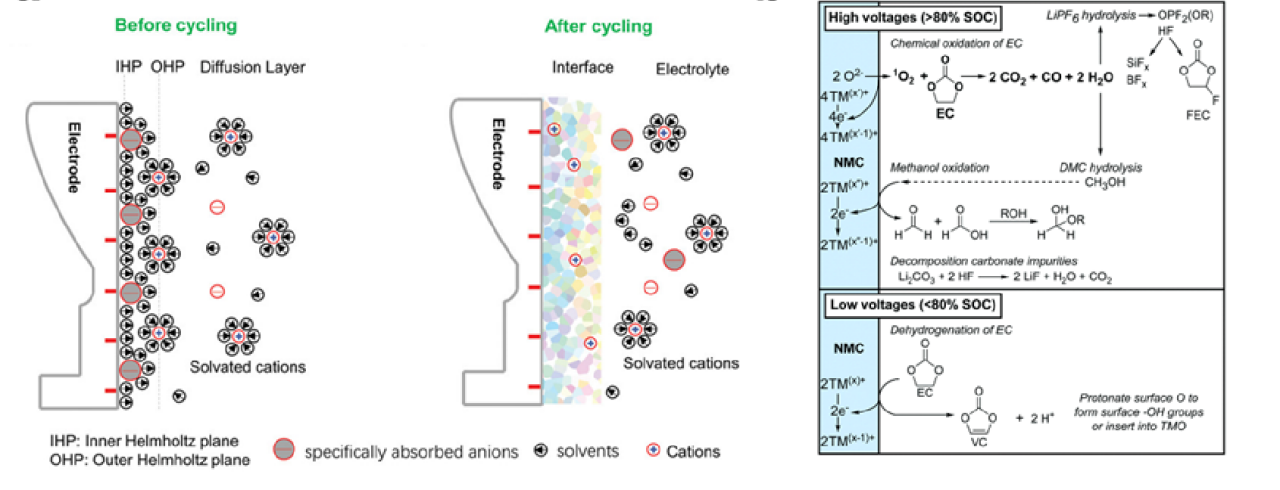
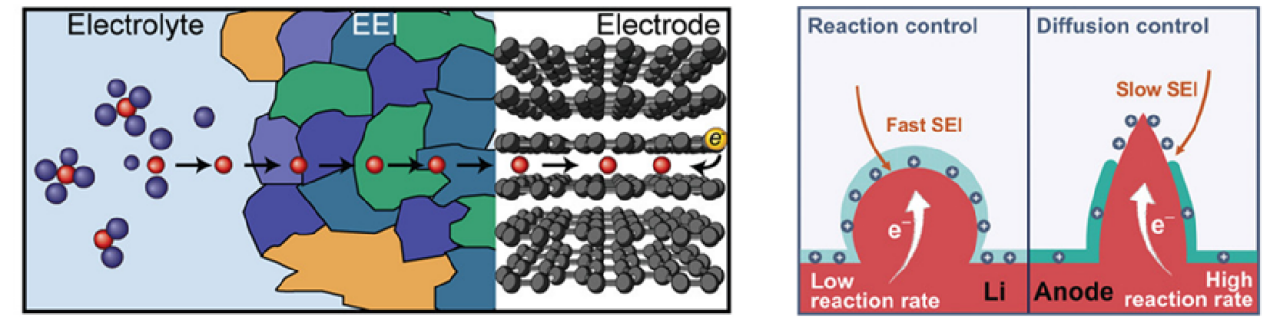 图3. SEI/CEI膜的形成机理及离子输运特性
图3. SEI/CEI膜的形成机理及离子输运特性
界面双电层的形成与结构主要受库仑力、电极表面的化学相互作用以及熵驱动。如图3所示,与电极表面相互作用强的离子或分子通过偶极矩或其它化学作用力吸附在电极最表面的IHP,并倾向于失去部分或者全部的溶剂化分子。在OHP中,离子也主要以溶剂化的形式存在,且随着与电极距离的增加浓度逐渐降低。当电池开始循环时,形成的电子绝缘的SEI/CEI膜将取代IHP层的特异性吸附。由于双电层的形成时间极短,约为10-8s,远小于电解液发生氧化还原反应的时间(10-2~10-4s),电极表面初始的竞争性吸附是决定SEI/CEI膜的初始化学组成与结构的关键因素。尽管在IHP吸附的大部分离子是去溶剂化的,但是它的组成也与电解液的溶剂化结构密切相关。电解液中的阳离子(L、Na等)是强路易斯酸,与溶剂分子有较强的配位趋势,不容易去溶剂化;而阴离子由于其分子轨道与溶剂分子匹配较难,难以形成溶剂化结构。因此,即使电极带负电,阴离子也比阳离子更容易在电极表面形成特异性吸附。尤其是当电解液中的盐浓度升高时,游离的溶剂分子减少,溶剂分子的特异性吸附将被抑制,大量阴离子会吸附在IHP并在循环过程中优先分解形成富含无机物的SEI膜。电解液的分解路径与温度、电位、电流、电解液组分以及电极材料等密切有关。通过对电解质分解产物的检测,可反推其反应机理。Rinkel等人利用在线电化学质(OEMS)和NMR检测了1molL-1LiPF。EC/DMC电解液在NCM正极材料表面分解产生的气体与可溶性分解产物,由此提出了电解液在不界面双电层的形成与结构主要受库仑力、电极表面的化学相互作用以及熵驱动。如图3所示,与电极表面相互作用强的离子或分子通过偶极矩或其它化学作用力吸附在电极最表面的IHP,并倾向于失去部分或者全部的溶剂化分子。在OHP中,离子也主要以溶剂化的形式存在,且随着与电极距离的增加浓度逐渐降低。当电池开始循环时,形成的电子绝缘的SEI/CEI膜将取代IHP层的特异性吸附。由于双电层的形成时间极短,约为10-8s,远小于电解液发生氧化还原反应的时间(10-2~10-4s)。
电极表面初始的竞争性吸附是决定SEI/CEI膜的初始化学组成与结构的关键因素。尽管在IHP吸附的大部分离子是去溶剂化的,但是它的组成也与电解液的溶剂化结构密切相关。电解液中的阳离子(L、Na等)是强路易斯酸,与溶剂分子有较强的配位趋势,不容易去溶剂化;而阴离子由于其分子轨道与溶剂分子匹配较难,难以形成溶剂化结构。因此,即使电极带负电,阴离子也比阳离子更容易在电极表面形成特异性吸附。尤其是当电解液中的盐浓度升高时,游离的溶剂分子减少,溶剂分子的特异性吸附将被抑制,大量阴离子会吸附在IHP并在循环过程中优先分解形成富含无机物的SEI膜。电解液的分解路径与温度、电位、电流、电解液组分以及电极材料等密切有关。通过对电解质分解产物的检测,可反推其反应机理。Rinkel等人利用在线电化学质谱(OEMS)和NMR检测了1molL-1LiPF6 EC/DMC电解液在NCM正极材料表面分解产生的气体与可溶性分解产物,由此提出了电解液在不同电位下的分解机理。在低电位下,EC在正极表面脱H形成碳酸亚乙烯酯(VC)。而在高电位下,正极晶格中释放的1O2将EC氧化为CO2、CO和H2O。随后,H2O将引发一系列反应:(i)H2O首先与LiPF6反应生成氟磷酸盐和HF,HF进一步与VC反应形成FEC;(ii)DMC缓慢水解形成甲醇,然后又被氧化为甲醛和甲酸;最后在H2O和甲醇的作用下,甲醛缩合形成缩醛。部分正极侧的分解产物还会扩散到负极产生串扰效应。此外,Hoz等人使用密度泛函理论和分子动力学模拟分析了FEC在LixSi表面的还原机制,发现FEC的分解速度很快,基本与电极锂化程度无关。FEC可能有三种还原机制,其中一种机制为FEC脱去一个H和F形成VC2-阴离子,此时FEC和VC的还原产物可能完全相同;而在另外两种机制中,FEC经过四电子还原过程分别形成CO22-、F、CH2CHO或CO2-、F、·CH2CHO,这些产物还会进一步聚合形成低聚物。这三种机制都会形成L,与实验观察结果一致。总之,申解液的分解反应非常复杂,需要不断地发展新的表征方法,全面地分析分解产物,才能加深对电解液分解反应的认识。